Canxi rất quan trọng để duy trì cấu trúc thành tế bào, nơi nó liên kết chéo các pectin ở lớp giữa, cũng như cho tính toàn vẹn của màng và các quá trình truyền tín hiệu. Tuy nhiên, khi bón lá, Ca phải đối mặt với một số nút thắt sinh lý và thể chất.
Bởi vì Ca được vận chuyển chủ yếu qua xylem và có khả năng di chuyển phloem rất hạn chế (White, 2001), quả đang phát triển - thường có dòng thoát hơi nước yếu - được cung cấp kém. Sau khi xâm nhập, Ca²⁺ liên kết mạnh mẽ trong apoplast, hạn chế sự phân bố lại và di chuyển vào các mô sâu hơn (Hocking et al., 2016).
Hơn nữa, lớp biểu bì và lớp biểu bì có những rào cản đáng kể đối với sự xâm nhập, đặc biệt là khi các chất tan ion như Ca²⁺ yêu cầu hydrat hóa bề mặt mở rộng và các con đường phân cực cụ thể để khuếch tán hiệu quả (Fernández & Brown, 2013). Những hạn chế này giải thích tại sao hiệu quả của thuốc xịt Ca qua lá thường phụ thuộc vào việc sử dụng nhiều lần, độ che phủ trực tiếp của quả và điều kiện môi trường thuận lợi kéo dài độ ẩm của giọt bắn.
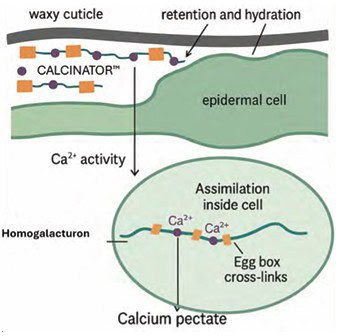
Con đường hấp thu
canxi qua lá Sự xâm nhập của Ca vào lá và quả được chi phối bởi sự giữ lại của giọt, thời gian hydrat hóa và cấu trúc vi mô biểu bì. Độ ẩm giọt kéo dài thúc đẩy sự khuếch tán của các ion qua các miền ưa nước của lớp biểu bì và thành tế bào biểu bì. Sự hấp thu khí khổng có thể góp phần vào lá nhưng có liên quan hạn chế trong vỏ quả, nơi khí khổng trở nên không hoạt động khi tiến triển (Eichert & Goldbach, 2008).
Ở trái cây, sự hấp thu xảy ra chủ yếu thông qua các miền vi mô cực, các vết nứt nhỏ trên bề mặt và mối nối cuống - quả, tất cả đều được xác định là điểm nóng hấp thụ Ca (Winkler và cộng sự, 2021; Hurtado và cộng sự, 2025).
Những phát hiện này nhấn mạnh rằng phun trực tiếp lên bề mặt trái cây, đặc biệt là tại các điểm xâm nhập nhạy cảm, là rất quan trọng để phân phối Ca hiệu quả.
Cơ sở cơ học cho công thức canxi-pectate
Một công thức phức hợp canxi-carbohydrate như CALCINATOR™ được thiết kế để khắc phục nhiều thiếu sót của thuốc xịt canxi thông thường (Hình 1). Trong hệ thống này, các ion Ca²⁺ được phức hợp với các cacboxylat trọng lượng phân tử thấp, tạo ra phức hợp đệm và ưa nước với các tính chất hóa lý đặc biệt. Bản chất tạo gel của phối tử pectic làm tăng độ nhớt và độ ẩm của giọt, giúp tăng cường độ bám dính vào vỏ trái cây, giảm sự phục hồi của giọt và kéo dài thời gian hydrat hóa (Blanco và cộng sự, 2010).
Bằng cách điều chỉnh hoạt động ion tại giao diện, nhiều Ca có thể khuếch tán vào apoplast trước khi trở nên bất động. Khi vào bên trong, Ca²⁺ dần dần được giải phóng khỏi phức hợp và kết hợp vào các chuỗi đồng tính nội sinh bên trong lam giữa, tạo thành các liên kết chéo canxi-pectate được gọi là cấu trúc "hộp trứng". Các liên kết chéo này củng cố thành tế bào, giảm rò rỉ màng và làm chậm quá trình hòa tan pectin, do đó cải thiện độ cứng của quả và giảm rối loạn sinh lý ( Huang và cộng sự, 2023 ).
So với các muối hòa tan cao như CaCl₂, cung cấp tải trọng thẩm thấu cao, công thức CALCINATOR™ cung cấp Ca nhẹ nhàng hơn, giảm nguy cơ cháy muối và cung cấp khả năng tương thích rộng hơn trong hỗn hợp bể (Wójcik et al., 2014).
So sánh với các nguồn
canxi khác Muối canxi không phức tạp như CaCl₂ và Ca(NO₃)₂ có hiệu quả trong việc tăng hàm lượng Ca trong quả khi được áp dụng trong điều kiện thuận lợi. Tuy nhiên, chúng có liên quan đến những hạn chế đáng kể, bao gồm nguy cơ độc tính thực vật cao, đặc biệt là trong điều kiện ấm áp, khô chậm và thường xuyên không tương thích trong hỗn hợp bể do kết tủa với phốt phát và sunfat (Autio & Schupp, 2001; Wójcik và cộng sự, 2014).
Mặc dù chúng có thể cung cấp một lượng lớn Ca một cách nhanh chóng, nhưng hiệu suất của chúng không nhất quán và phụ thuộc nhiều vào điều kiện môi trường. Hỗn dịch cô đặc (SC) của các nguồn Ca hòa tan ít như CaCO₃ hoạt động khác nhau. Các công thức này lắng đọng các hạt trên bề mặt lá hoặc quả, nơi sự hòa tan dần dần giải phóng Ca theo thời gian.
Mặc dù SC có thể cung cấp các lợi ích phản chiếu và bảo vệ gián tiếp hỗ trợ sinh lý trái cây, nhưng đóng góp dinh dưỡng của chúng bị hạn chế bởi tốc độ hòa tan chậm của các hợp chất này trong điều kiện đồng ruộng (Pimentel et al., 2023). Ngược lại, CALCINATOR™ cung cấp cả sự đồng hóa nhanh chóng và có liên quan đến sinh hóa của Ca vào các mô quả, ưu tiên tác động dinh dưỡng trực tiếp hơn điều hòa bề mặt.
Quá trình hấp thu, chuyển vị và đồng hóa canxi-pectate
Quá trình hấp thu của CALCINATOR™ bắt đầu bằng việc lắng đọng các giọt bám chặt vào bề mặt quả và duy trì ngậm nước trong thời gian dài. Trong các giọt này, các phức Ca²⁺ đệm khuếch tán qua các đường biểu bì cực và các vết nứt nhỏ. Khi ở bên trong lớp biểu bì và apoplast, sự chuyển vị xảy ra chủ yếu trong khoảng cách ngắn, vì Ca phần lớn vẫn bất động trong symplast và phloem (White, 2001).
Sự phân phối cục bộ này nhấn mạnh tầm quan trọng của việc phun trái cây trực tiếp lặp đi lặp lại. Bước đồng hóa rất quan trọng: Khi các ion Ca²⁺ phân ly khỏi phối tử, chúng liên kết với các khối đồng galacturonan trong thành tế bào, tạo thành các liên kết chéo canxi-pectate giúp tăng độ cứng và khả năng chống phân hủy ( Huang và cộng sự, 2023 ).
Kết luận
Các công thức bón lá canxi-pectate như CALCINATOR™ đại diện cho một cách tiếp cận hợp lý về mặt khoa học để giải quyết những thách thức dai dẳng của dinh dưỡng canxi lá trong cây ăn quả. Bằng cách kết hợp việc giữ giọt kéo dài và hoạt động ion đệm với sự đồng hóa có mục tiêu vào pectin thành tế bào, các công thức này cải thiện hiệu quả đồng thời giảm nguy cơ bỏng muối và mở rộng khả năng tương thích.
So với muối không phức tạp, chúng cung cấp Ca nhẹ nhàng và đáng tin cậy hơn, đồng thời mang lại lợi ích dinh dưỡng mạnh mẽ hơn so với hỗn dịch cô đặc. Cuối cùng, thành công vẫn phụ thuộc vào độ che phủ trực tiếp của trái cây lặp đi lặp lại và thời gian môi trường thuận lợi, nhưng các công thức canxi-pectate đại diện cho một tiến bộ có ý nghĩa trong việc tối ưu hóa tình trạng Ca của trái cây và giảm các rối loạn liên quan đến canxi.
Tài liệu tham khảo:
1. Autio W, Schupp J (2001/2012). Thuốc xịt canxi lá cho táo (F-119R). Đại học Massachusetts / Đại học Vermont.
2. Blanco A, và cộng sự (2010). Cải thiện hiệu suất của các công thức xịt chứa canxi. Scientia Horticulturae 125.
3. Eichert T, Goldbach HE (2008). Bán kính lỗ rỗng tương đương của các tuyến hấp thụ lá ưa nước. Thực vật, Tế bào và Môi trường 31: 1299–1309.
4. Fernández V, Brown PH (2013). Từ bề mặt thực vật đến quá trình trao đổi chất của cây. Biên giới trong Khoa học Thực vật 4: 289.
5. Hocking B, Tyerman SD, Burton RA, Gilliham M (2016). Canxi trái cây: vận chuyển và sinh lý. Biên giới trong Khoa học Thực vật 7: 569.
6. Huang W, và cộng sự (2023). Phức hợp homogalacturonan qua trung gian canxi góp phần tạo nên độ săn chắc ở mướp. Tạp chí Nghiên cứu Cao cấp 49: 47–62.
7. Hurtado G, và cộng sự (2025). Con đường và các yếu tố hấp thu canxi qua vỏ dâu tây. Báo cáo khoa học 15.
8. Hu Y, và cộng sự (2023). Biên tập: Các yếu tố ảnh hưởng đến hiệu quả của phân bón lá. Biên giới trong Khoa học Thực vật 14:1121806.
9. Pimentel C, và cộng sự (2023). Các hạt khoáng trong công thức phân bón lá. Cây trồng 12.
10. PJ trắng (2001). Các con đường chuyển động của canxi đến xylem. Tạp chí Thực vật học Thực nghiệm 52: 891–899.
11. Winkler A, và cộng sự (2021). Hấp thu canxi qua vỏ quả anh đào ngọt ngào. Scientia Horticulturae 283: 110059.
12. Wójcik P, và cộng sự (2014). Thuốc phun CaCl2 trước khi thu hoạch vào chất lượng táo và tổn thương lá. Scientia Horticulturae 171: 46–51.
13. Yamane T (2014). Ứng dụng canxi lá trên cây ăn quả rụng lá: tổng quan. JARQ 48 (1): 25–31.