Sản xuất thành công sản phẩm IL-2 tái tổ hợp hỗ trợ điều trị ung thư
Xây dựng được hệ thống chủng giống cho sản xuất IL-2 tái tổ hợp trên dòng tế bào E.coli; xây dựng quy trình công nghệ sản xuất IL-2 tái tổ hợp trên dòng tế bào E.coli ở quy mô bán công nghiệp và sản xuất 3 loạt IL-2 liên tiếp ở quy mô bán công nghiệp (15.000 liều/loạt) theo quy trình công nghệ xây dựng được;…
PGS.TS
Đoàn Thị Thủy, Chủ nhiệm Dự án trình bày báo cáo kết quả Dự án (Ảnh: Hạnh
Nguyên)
Đây là kết quả nổi bật của Dự án KC.04.DA02/11-15 “Hoàn
thiện quy trình công nghệ sản xuất Interleukin-2 tái tổ hợp trên dòng tế bào E.
coli”, mã số KC.04.DA02/11-15 do PGS.TS Đoàn Thị Thủy, Phó Giám đốc Công ty
TNHH MTV Vắc-xin và Sinh phẩm số 1 (VABIOTECH) làm chủ nhiệm, Viện Công nghệ
Sinh học cùng phối hợp thực hiện. Thông tin trên được đưa ra tại buổi họp Hội đồng
đánh giá nghiệm thu cấp Nhà nước do Ban Chủ nhiệm Chương trình khoa học và công
nghệ (KH&CN) trọng điểm cấp nhà nước giai đoạn 2011-2015 “Nghiên cứu ứng dụng
và phát triển công nghệ sinh học (KC.04/11-15)” và Văn phòng Các chương trình
trọng điểm cấp nhà nước (Bộ KH&CN) tổ chức ngày 26/11/2015, tại Hà Nội.
Dự án này là sự tiếp nối của 2 đề tài KH&CN cấp nhà
nước do Viện Công nghệ Sinh học chủ trì “Nghiên cứu tạo Interleukin-2 tái tổ hợp
dùng cho điều trị ung thư” (mã số KC.04.33), giai đoạn 2005-2007 và “Nghiên cứu
đánh giá hiệu lực Interleukin-2 tái tổ hợp sản xuất tại Việt Nam dùng trong hỗ
trợ điều trị ung thư” (mã số KC.04-21/06-10), giai đoạn 2009-2010. Kết quả nghiệm
thu cho thấy, các đề tài đã tạo được quy trình chuẩn để sản xuất thử nghiệm 5.000
liều sản phẩm IL-2 người tái tổ hợp. Tuy nhiên, do thời gian thực hiện đề tài
có hạn, chất lượng sản phẩm (Bảng tiêu chuẩn cơ sở) cần được hoàn thiện hơn để
đáp ứng các tiêu chuẩn quy định chặt chẽ của một sản phẩm dùng cho người nên Dự
án KC.04.DA02/11-15 “Hoàn thiện quy trình công nghệ sản xuất Interleukin-2 tái
tổ hợp trên dòng tế bào E. coli” đã được triển khai.
Sau quá trình triển khai thực hiện (01/01/2012 -
01/09/2015), đến nay Dự án đã xây dựng được hệ thống chủng giống cho sản xuất
IL-2 tái tổ hợp trên dòng tế bào E.coli, hệ thống chủng giống gồm 300 ống chủng
gốc giống (MCB), 300 ống chủng sản xuất (WCB) và xây dựng bảng tiêu chuẩn cơ sở
cho hệ thống chủng giống; hoàn thiện quy trình công nghệ sản xuất IL-2 tái tổ hợp
dựa trên quy trình công nghệ tiếp nhận từ đề tài KC.04.21/06-10, xây dựng được
quy trình công nghệ sản xuất IL-2 tái tổ hợp trên dòng tế bào E.coli ở quy mô
bán công nghiệp; xây dựng các phương pháp kiểm định và bảng tiêu chuẩn cơ sở
cho chế phẩm IL-2 tái tổ hợp; sản xuất 03 loạt IL-2 liên tiếp ở quy mô bán công
nghiệp (15.000 liều/loạt) đạt tiêu chuẩn 300.000IU/liều theo quy trình công nghệ
xây dựng được.
Nhóm nghiên cứu cũng đã kiểm tra chất lượng 03 loạt IL-2
theo 10 tiêu chuẩn cơ sở đã xây dựng. Cả 3 loạt đều đạt các tiêu chuẩn chấp thuận
về cảm quan, độ ẩm tồn dư, pH, nội độc tố, hàm lượng protein, hoạt tính sinh học,
vô trùng, chí nhiệt tố trên thỏ, an toàn chung và độ tinh sạch.
Theo PGS.TS Đoàn Thị Thủy, Chủ nhiệm Dự án, khi được phép
sản xuất và đưa ra thị trường, người bệnh sẽ được hưởng lợi do sản phẩm có chất
lượng tốt, giá thành hạ so với sản phẩm nhập ngoại. Theo ước tính sơ bộ của dự
án, sản phẩm IL-2 có giá khoảng 150 ngàn đồng/liều (300.000 IU) và sau này đưa
vào sản xuất giá thành sẽ còn thấp hơn, trong khi IL-2 của Trung Quốc có giá
210 ngàn đồng/liều khi nhập về Việt Nam. Việc chủ động tạo được sản phẩm IL-2
tái tổ hợp theo hướng công nghệ cao trong nước với giá thành thấp hơn thế giới
để ứng dụng trong điều trị bệnh ung thư sẽ giúp giảm bớt hiện tượng nhập siêu
các sản phẩm sử dụng trong y tế tại Việt Nam.
|
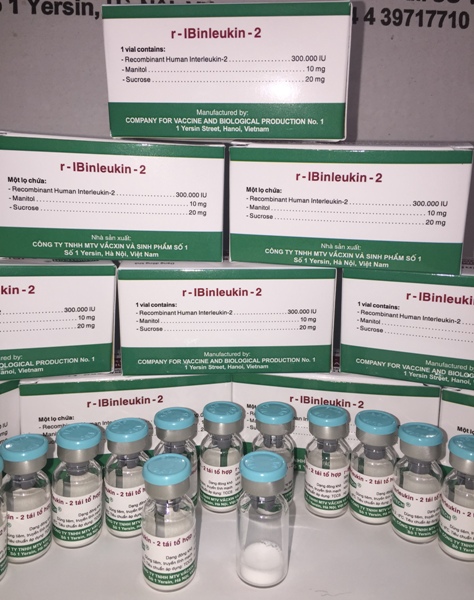
Sản
phẩm của Dự án (Ảnh: Hạnh Nguyên) |
Tại buổi nghiệm thu, các thành viên Hội đồng đều đánh giá
rất cao những kết quả đạt được của nhóm nghiên cứu. Hội đồng đã nhất trí thông
qua và đánh giá Dự án xếp loại Xuất sắc. Đồng thời kiến nghị Dự án cần được tiếp
tục đầu tư nghiên cứu, thử nghiệm tiền lâm sàng trên động vật thực nghiệm, tiến
hành các thủ tục cần thiết để được thử nghiệm lâm sàng trên bệnh nhận tình nguyện
nhằm đánh giá tính an toàn và hiệu quả điều trị của sản phẩm,...