Xây dựng quy trình phân tích đồng thời phenylephrin, acid ascorbic, paracetamol, cafein trong viên nén bao phim bằng phương pháp HPLC/PDA và ứng dụng khảo sát ảnh hưởng của nhiệt độ, độ ẩm đến độ ổn định hàm lượng hoạt chất
Nghiên cứu do hai tác giả Ngô Thị Phương Ánh,Đỗ Châu Minh Vĩnh Thọ thực hiện.
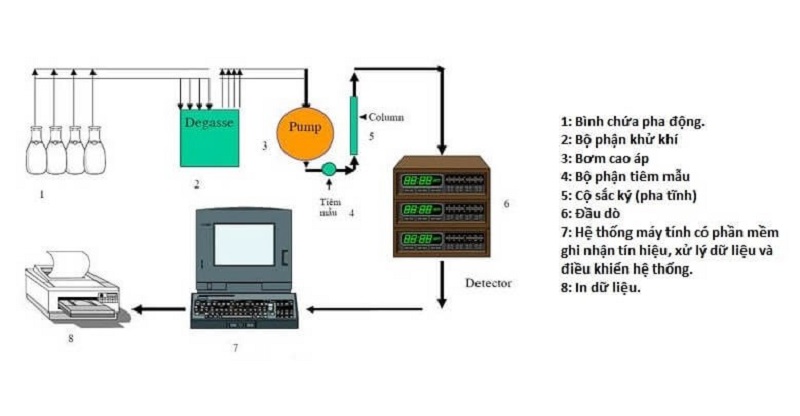
Hình ảnh minh họa
Yêu cầu quan trọng và bắt buộc đối với thành phẩm thuốc là phải đảm bảo an toàn, hiệu lực và chất lượng thuốc từ khâu sản xuất, bảo quản và lưu thông, phân phối đến khi hết hạn dùng. Do đó, khi nghiên cứu đưa ra thị trường một chế phẩm thuốc, bên cạnh các nghiên cứu định tính, định lượng để xác định hàm lượng hoạt chất, thì việc ứng dụng quy trình định lượng để khảo sát, đánh giá ảnh hưởng của các yếu tố môi trường như: nhiệt độ, độ ẩm, ánh sáng đến độ ổn định của chế phẩm là một yêu cầu rất quan trọng và không thể thiếu trong nghiên cứu độ ổn định của thuốc. Chế phẩm viên nén bao phim phối hợp 04 hoạt chất phenylephrin, acid ascorbic, cafein, paracetamol giúp bệnh nhân giảm số thuốc phải dùng, giảm phản ứng có hại của thuốc (ADR) và hiệp lực nhiều tác dụng điều trị đang được sử dụng ngày càng phổ biến trên thị trường. Tuy nhiên, hiện nay chỉ có một vài công trình nghiên cứu định lượng đồng thời chế phẩm chứa 4 hoạt chất này bằng phương pháp HPLC-UV/VIS, vẫn chưa có quy trình định lượng đồng thời bốn hoạt chất này bằng phương pháp sắc ký lỏng ghép nối đầu dò dãy diod quang (cho phép quét và so phổ UV-Vis để nâng cao độ đặc hiệu về mặt định tính pic và đánh giá tinh khiết pic) trong các tài liệu chính tắc như Dược điển Việt Nam 5, Dược điển Anh (BP 2019), Dược điển Mỹ (USP 41). Do đó, việc xây dựng quy trình định lượng đồng thời phenylephrin, acid ascorbic, paracetamol, cafein bằng phương pháp sắc ký lỏng hiệu năng cao ghép nối đầu dò dãy diod quang và ứng dụng để khảo sát, đánh giá ảnh hưởng của nhiệt độ, độ ẩm đến độ ổn định của chế phẩm trong nghiên cứu qui mô pilot là một nhu cầu rất cần thiết.
Đối tượng nghiên cứu
Mẫu viên nén bao phim:Paracetamol 400 mg, cafein 30 mg, phenylephrin HCl 5 mg, acid ascorbic 50 mg, tá dược vừa đủ 665 mg.
Phương pháp nghiên cứu
Khảo sát điều kiện sắc ký: Dựa vào cấu trúc hóa học của các hoạt chất nghiên cứu với giá trị pKa > 4,5 với độ phân cực từ trung bình đến phân cực, và các tài liệu tham khảo.
Chuẩn bị mẫu: Mẫu dung dịch hỗn hợp chuẩn và mẫu thử viên nén bao phim
Kết luận
Qui trình phân tích đồng thời phenylephrin, acid ascorbic, cafein, paracetamol trong mẫu viên nén bao phim bằng phương pháp sắc ký lỏng hiệu năng cao ghép nối đầu dò dãy diod quang đã được xây dựng và thẩm định đạt yêu cầu theo quy định của ICH. Quy trình có tính đặc hiệu, độ nhạy cao, cho kết quả đúng và chính xác. Quy trình được ứng dụng để khảo sát, đánh giá độ ổn định hàm lượng của 4 hoạt chất trong viên nén bao phim nghiên cứu qui mô pilot ở điều kiện nhiệt độ 40 °C ± 2 °C, độ ẩm 75 % ± 5 % trong 6 tháng và nhiệt độ 30 °C ± 2 °C, độ ẩm 75 % ± 5 % trong 12 tháng nghiên cứu. Kết quả thực nghiệm được vận dụng để ước lượng tuổi thọ của viên nén bao phim chứa PHE, ASC, PAR, CAF qui mô nghiên cứu pilot là 438 ngày.
Tạp chí y dược học, Tập. 60 Số. 4(2020)